فارماکوژنومیکس
فارماكوژنومیكس مطالعه چگونگی تأثیر ژن ها در پاسخ فرد به داروها است.این رشته نسبتاً جدید ترکیبی از داروشناسی (علم داروها) و ژنومیک (مطالعه ژن ها و عملکرد آنها) است تا داروهای موثر و بی خطر و متناسب با ترکیب ژنتیکی فرد ایجاد کند.
این شاخه امروزه کاربرد وسیعی در پزشکی شخصی سازی شده (Personalized Medicine ) دارد.
هدف از پزشکی شخصی سازی شده،مناسب سازی درمان برای هر شخص یا گروهی از افراد است.در این علم با بررسی DNA شما،نحوه پاسخ بدن شما به داروها مشخص می گرددو می توان مناسب ترین دارو را برای هر فرد انتخاب نمود.در برخی موارد،اطلاعات ژنتیکی شما می تواندمشخص نماید که آیا شما پاسخ نادرستی به دارو خواهیدداشت و یا آن دارو می تواند بدون هیچگونه اثرات جانبی دارویی (ADR) به شما کمک نماید.
درحال حاضر برای درمان یک بیماری،به همه بیماران مربوطه با هر جنس وژنتیکی یک نوع دارو بادوز یکسان داده می شود،مشکل این است که این دوز فقط برای 60 درصد بیماران مناسب است،درنتیجه 40 درصد از جمعیت در معرض خطر عوارض جانبی دارویی مرتبط با پلی مورفیسم ژنتیکی قرار دارند.
فارماکوژنومیکس این امکان را فراهم می کندتا ژن های درگیر در متابولیسم دارو را مورد مطالعه قرار داده و ازین طریق مشخص شود که آیا این دارو برای بیمار مضر است یا خیر و درنهایت درمان مناسب رابرای او فراهم کند.
فارماکوژنومیکس با تأثیر تنوع ژنتیکی اکتسابی و ارثی بر پاسخ به دارو در بیماران از طریق همبستگی بیان ژن یا چندشکلی تک نوکلئوتیدی با فارماکوکینتیک (جذب دارو ، توزیع ، متابولیسم و از بین بردن دارو) و فارماکودینامیک (اثرات ناشی از اهداف بیولوژیکی دارو) سروکار دارد.
برای آشنایی بیشتر توضیح مختصری درمورد فارماکوکینیتیک و فارماماکودینامیک میدهیم:
فارماکودینامیک به مطالعه اثر داروها بربدن و فارماکوکینیتیک به اثر و رفتار بدن بر روی داروها میگویند.برای بررسی فارماکوکینیتیک با استفاده از پایگاه داده های مشخص ترکیب دارویی بدست آورده با ترکیب های موجود دیگر مقایسه می شود و فارماکوکینیتیک دارای فاکتور های جذب ،توزیع،متابولیسم،دفع و سمیت را بررسی میکند که ADMET نام اختصاری فاکتور ها میباشد.
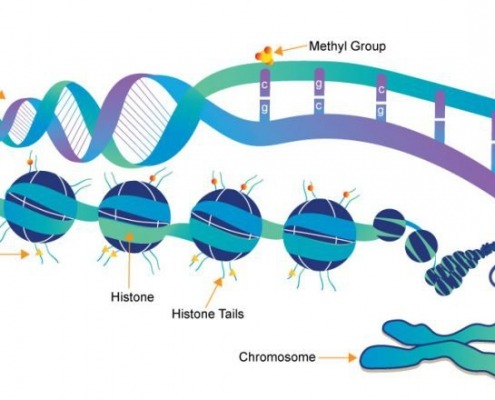
اصطلاح فارماكوژنوميك غالباً با فارماكوژنتيك به كار رفته می شود، اگرچه هر دو اصطلاح مربوط به پاسخ دارو بر اساس تأثیرات ژنتیکی است،با این حال فارماکوژنتیک بر فعل و انفعالات منفرد ژن دارویی متمرکز است ، در حالی که فارماکوژنومیک شامل یک رویکرد ارتباطی در ژنوم گسترده تر است،اگر با ژنومیک و اپی ژنتیک ترکیب شودبا اثرات چندین ژن در پاسخ به دارو روبرو می شود.
هدف از فارماكوژنومیكس آن است كه روش های منطقی برای بهینه سازی درمان دارویی،با توجه به ژنوتیپ بیماران،برای اطمینان از حداكثر كارآیی با حداقل اثرات سو ایجاد كند.
با استفاده از فارماكوژنوميکس،اميداست كه درمان هاي دارويي پیشین که رويكرد “يك دوز براي همه” ناميده مي شود،کنارگذاشته شود،همچنین تلاش می کند روش تجویز خطا و آزمایشی را از بین ببردوبه پزشكان اجازه می دهد تابا بررسی ژن های بیمار خود،كاركرد ژن های بیمارو چگونگی اثربخشی درمان های فعلی یاآتی بیمار را در نظر بگیرندودر صورت نیاز،توضیحی در مورد عدم موفقیت در درمان های گذشته ارائه دهد.
بابررسی بیش از پیش فارماکوژنومیکس می توان انتظار داروی دقیق وحتی داروی شخصی را داشت ویا برای بیمارانی که فاقد پاسخ به درمان هستند،می توان روش های درمانی جایگزین را که با نیازهای آنها متناسب است،تجویز کرد.
امیداست که نتایج بهتر درمانی،اثربخشی بیشتر،به حداقل رساندن سمیت دارویی و واکنش های جانبی دارو با کمک فارماکوژنومیکس یافته شود.











Thanks for the good article, I hope you continue to work as well.Спаситель на продажу
Thank you for attention